近日,必赢官网郭媛教授/张健健教授团队在糖尿病并发药物性肝损伤(DILI)的诊疗一体化研究中取得重要进展。该团队成功构建了一种羧酸酯酶(CE)激活型硫化氢(H₂S)供体(SKCLS)分子药物策略,该策略同时集成了近红外荧光(NIRF)与化学发光(CHL)双模态成像功能,可实现对糖尿病小鼠模型中DILI进程的精准可视化监测与有效治疗,为临床解决糖尿病用药所致肝毒性问题提供了新的方案。
糖尿病作为全球性代谢疾病,其长期药物治疗(如二甲双胍、阿卡波糖等)常伴随剂量依赖性的肝损伤风险,特别是药物性肝损伤。当前用于诊断DILI的成像方式,例如计算机断层扫描(CT)、磁共振成像(MRI)和对比增强超声(CEUS)在灵敏度、成本及辐射暴露等方面存在局限。荧光成像凭借高灵敏度与时空分辨率,成为监测DILI的理想手段,其中近红外荧光更具备深层穿透与低毒性优势。然而,肝脏高代谢引发的自发荧光干扰限制了其精准度。化学发光无需激发光,彻底消除背景干扰并实现超高信噪比,却受限于光子产率低和持续时间短。为此,构建协同NIRF与CHL的双模态探针成为关键策略。该模式有效互补单模态短板,克服了背景噪声与信号衰减难题,实现了对DILI病程更精准、持久的实时追踪与评估。
尽管光学成像在DILI研究中潜力巨大,但诊疗一体化平台仍显匮乏。H₂S作为新兴气体信号分子,能通过修饰Keap1激活Nrf2通路,发挥显著抗炎抗氧化及护肝作用。基于此,研究团队创新设计了SKCLS探针。该探针由三部分构成:高效的NIRF/CHL双模发射团、基于硫酯的H₂S释放单元以及CE特异性触发基团N,N-二甲氨基甲酰基。在肝脏高表达的羧酸酯酶作用下,SKCLS发生水解反应,同步释放近红外荧光信号、化学发光信号以及羰基硫(COS),后者在碳酸酐酶催化下迅速转化为具有细胞保护作用的H₂S。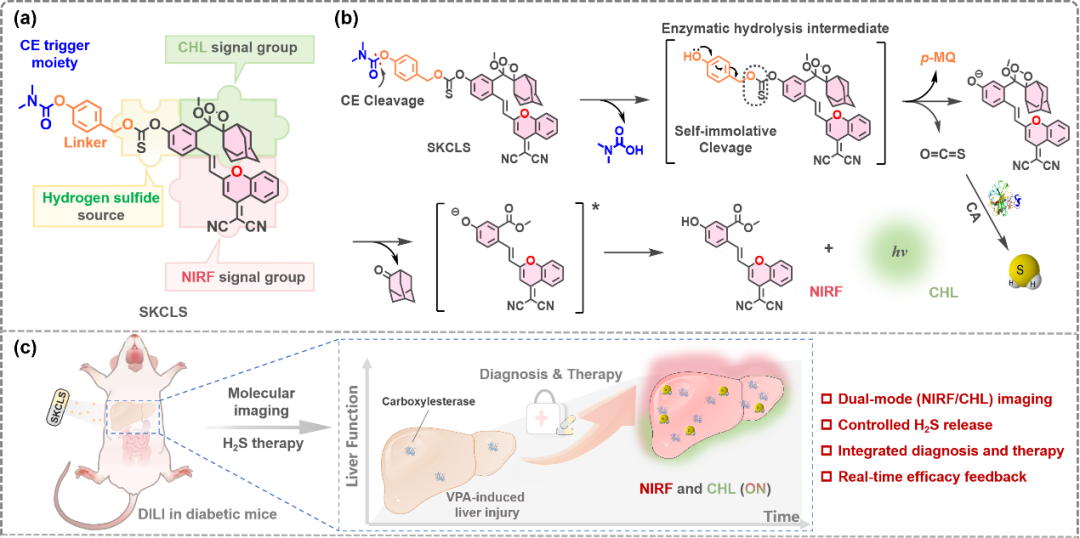

研究发现,SKCLS具有高灵敏度和选择性。体外实验显示,在CE存在下,其近红外荧光信号增强12倍,化学发光信号增强73倍,且不受其他生物分子干扰。在细胞层面,SKCLS成功区分了不同细胞系中CE的表达差异,并实时追踪了丙戊酸(VPA)诱导的肝毒性过程及其经抗氧化剂(NAC)干预后的修复动态。
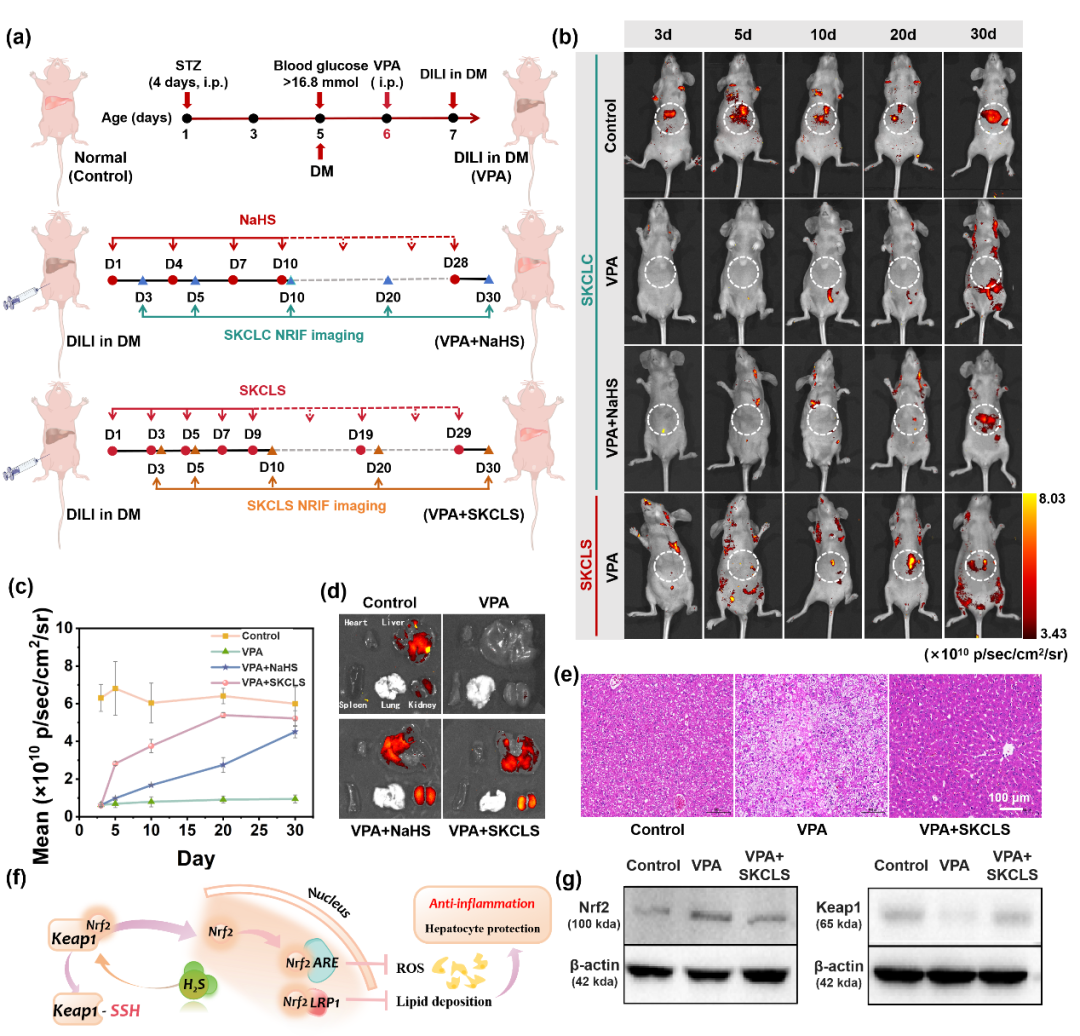
在糖尿病合并DILI的小鼠模型中,SKCLS展现了卓越的诊疗性能。双模态成像清晰揭示了VPA诱导的肝损伤导致CE活性显著抑制的现象,而经SKCLS治疗后,肝脏荧光信号随肝功能恢复而重现。借助SKCLS的诊疗一体化功能,该研究对接受不同剂量阿卡波糖与二甲双胍联用方案的小鼠肝脏进行了羧酸酯酶活性的实时追踪。监测结果清晰表明,给药剂量与肝损伤程度呈显著正相关。实验进一步证实,可控激活释放的H₂S在维持联用降糖药物降糖效果的同时,显著促进了受损肝功能的修复进程。
该成果以 “Hydrogen Sulfide Donor Featuring Dual-Modal Imaging for the Theranostic Management of Drug-Induced Liver Injury” 为题,发表于国际药学期刊Journal of Medicinal Chemistry。必赢官网硕士研究生王悦为论文第一作者,郭媛教授和张健健教授为共同通讯作者。该研究率先开发出用于糖尿病DILI诊疗的双模态成像H₂S药物供体,为肝损伤的精准诊疗提供了 “酶激活-双模成像-气体治疗” 的研究范式。该工作得到了国家自然科学基金项目 (22277098, 22477101, 22037002)、陕西省基础科学(化学、生物学)研究院项目 (22JHQ070) 及教育部心肌缺血重点实验室项目 (KF202311) 等支持。

